Salud mental y bienestar de los profesionales sanitarios
La salud mental de los profesionales sanitarios está influida por determinantes sociales y factores laborales. Es clave identificar riesgos y recursos, promover la equidad en el acceso a […]
El cambio de perspectiva permitirá obtener más información para proteger a los individuos más vulnerables y que tomen decisiones más seguras a la hora de medicarse

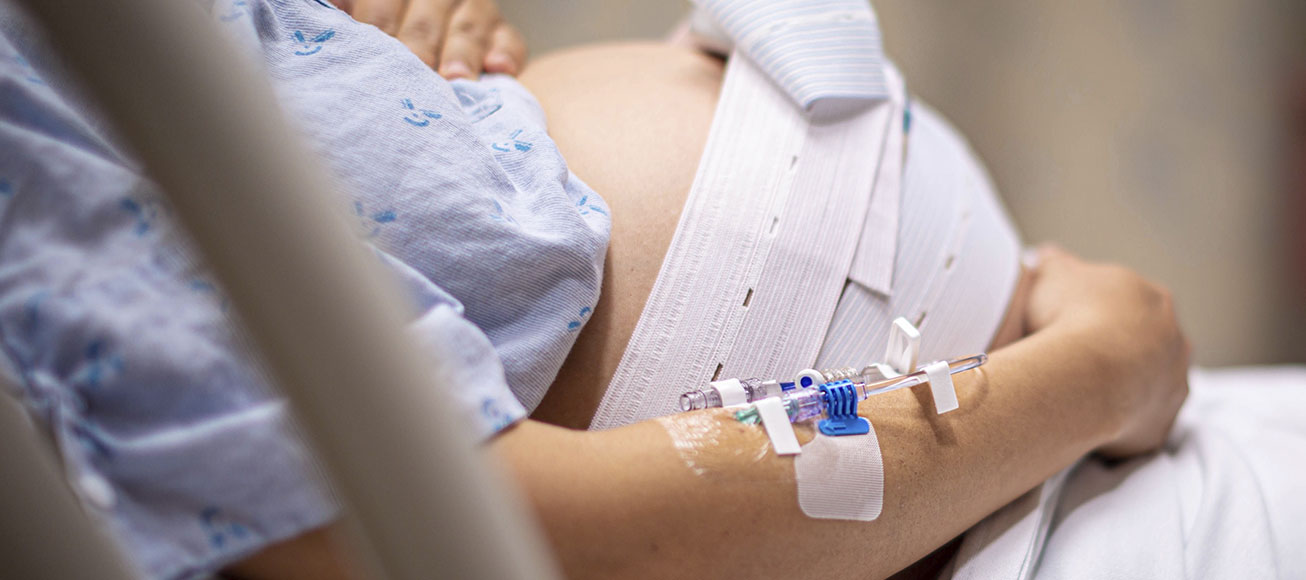
Tradicionalmente, la investigación clínica ha sido restrictiva con la participación de embarazadas y lactantes en los ensayos clínicos. En general, el embarazo y la lactancia se han tratado como variables de exclusión, no de estudio, debido a la necesidad de protegerlas de posibles efectos adversos1.
Sin embargo, este enfoque ha generado una brecha significativa de conocimiento sobre la seguridad y eficacia de ciertos tratamientos y situaciones peligrosas, ya que millones de mujeres toman medicamentos durante sus periodos de gestación y lactancia sin que existan evidencias sólidas sobre las posibles consecuencias.
Hasta el momento, el miedo al riesgo ha dejado a profesionales sanitarios y pacientes sin una parte del conocimiento terapéutico. Hoy en día, organismos y reguladores globales cuestionan esa lógica y exigen un cambio de paradigma ético y científico.
El Real Decreto 1090/2015, que regula los ensayos clínicos con medicamentos en España, estableció criterios de protección reforzada para colectivos vulnerables. Esta norma reconoce la necesidad de equilibrar el riesgo con el beneficio potencial, garantizando de manera clara la supervisión ética y el consentimiento informado1. En el caso de embarazadas o en periodo de lactancia también se debe cumplir con el artículo 33 del Reglamento europeo 536/20142.
En los últimos tiempos, la normativa vigente está experimentando una transformación profunda. En 2023, el Consejo Internacional para la Armonización de los Requisitos Técnicos para los Productos Farmacéuticos de Uso Humano (ICH, por sus siglas en inglés) aprobó una guía de eficacia para establecer un marco que permita sumar a mujeres embarazadas y en periodo de lactancia en ensayos clínicos3.
A mediados de este año, la Agencia Europea de Medicamentos (AEM) presentó esa guía E21, un documento desarrollado en colaboración con reguladores y la industria farmacéutica de todo el mundo, cuyo periodo de consultas terminó el 15 de septiembre4.
Este texto aboga por que se incluya a embarazadas y lactantes en todos los ensayos clínicos de medicamentos que estén destinados a poblaciones que puedan concebir cuando esté justificado por un beneficio científico y clínico. El objetivo es generar datos que permitan a médicos y pacientes tomar decisiones basadas en evidencias, no en suposiciones o extrapolaciones4.
Las directrices de la guía ICH E21 no solo animan a incorporar a estos colectivos, sino que detallan los principios científicos, éticos y regulatorios que se deben cumplir para garantizar la seguridad de todos los participantes: embarazadas, lactantes, fetos y bebés. Esto implica diseñar3:

La salud mental de los profesionales sanitarios está influida por determinantes sociales y factores laborales. Es clave identificar riesgos y recursos, promover la equidad en el acceso a […]
Por ejemplo, el desarrollo de una estrategia para recopilar datos relevantes para la lactancia se puede clasificar en los siguientes pasos5:
La adaptación de grupos de estudio para sumar a embarazadas en ensayos clínicos es una vía para avanzar en este ámbito6. Eso sí, al diseñar estos trabajos hay que preguntarse si7:
Las tendencias recientes muestran un impulso global sin precedentes. La Organización Mundial de la Salud (OMS) ha creado un grupo de trabajo mundial con la meta de lograr la inclusión de embarazadas y mujeres que amamantan en la investigación clínica para 20308.
Un análisis muestra que, de los ensayos clínicos registrados en el mundo durante la última década, solo el 4 % contaron con embarazadas, a pesar de que la mayoría de las mujeres toman al menos un medicamento prescrito mientras están encintas8.
Martina Penazzato, una de las responsables de investigación de la Red Global de Aceleradores para Formulaciones Pediátricas de la OMS (GAP-f), considera que “la inclusión ya no es una cuestión opcional y el paradigma debe cambiar”, ya que muchas mujeres con afecciones crónicas no saben si pueden continuar con sus tratamientos de manera segura cuando están embarazadas8.
Fuentes:
1. Boletín Oficial del Estado, Real Decreto 1090/2015, de 4 de diciembre, por el que se regulan los ensayos clínicos con medicamentos, los Comités de Ética de la Investigación con medicamentos y el Registro Español de Estudios Clínicos. https://www.boe.es/buscar/doc.php?id=BOE-A-2015-14082
2. Reglamento (UE) n °536/2014 del Parlamento Europeo y del Consejo, de 16 de abril de 2014, sobre los ensayos clínicos de medicamentos de uso humano https://eur-lex.europa.eu/legal-content/ES/TXT/?uri=CELEX:32014R0536
3. International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH), E21: Inclusion of Pregnant and Breast-feeding Individuals in Clinical Trials https://database.ich.org/sites/default/files/ICH_E21_Final_Concept_Paper_2023_1106_MCApproved.pdf
4. Agencia Europea de Medicamentos, New guideline on inclusion of pregnant and breastfeeding individuals in clinical trials https://www.ema.europa.eu/en/news/new-guideline-inclusion-pregnant-breastfeeding-individuals-clinical-trials
5. Agencia Europea de Medicamentos, ICH E21 Guideline on inclusion of pregnant and breastfeeding individuals in clinical trials https://www.ema.europa.eu/en/documents/other/ich-e21-guideline-inclusion-pregnant-breastfeeding-individuals-clinical-trials_en.pdf
6. Obstetric Medicine, Walking the walk to include pregnant participants in non-obstetric clinical trials: Insights from the SNAP Trial https://journals.sagepub.com/doi/10.1177/1753495X231163351
7. Journal of Obstetrics and Gynaecology Canada, Designing for Dyads: A multidisciplinary panel on inclusion of pregnant and lactating individuals and their infants in clinical trials https://www.jogc.com/article/S1701-2163(25)00357-3/fulltext
8. Organización Mundial de la Salud, Equidad y salud: la inclusión de las mujeres embarazadas y las mujeres que amamantan en los ensayos clínicos https://www.who.int/es/news/item/18-06-2025-equity-and-health–the-inclusion-of-pregnant-and-breastfeeding-women-in-clinical-trials
El cambio de perspectiva permitirá obtener más información para proteger a los individuos más vulnerables y que tomen decisiones más seguras a la hora de medicarse

Tradicionalmente, la investigación clínica ha sido restrictiva con la participación de embarazadas y lactantes en los ensayos clínicos. En general, el embarazo y la lactancia se han tratado como variables de exclusión, no de estudio, debido a la necesidad de protegerlas de posibles efectos adversos1.
Sin embargo, este enfoque ha generado una brecha significativa de conocimiento sobre la seguridad y eficacia de ciertos tratamientos y situaciones peligrosas, ya que millones de mujeres toman medicamentos durante sus periodos de gestación y lactancia sin que existan evidencias sólidas sobre las posibles consecuencias.
Hasta el momento, el miedo al riesgo ha dejado a profesionales sanitarios y pacientes sin una parte del conocimiento terapéutico. Hoy en día, organismos y reguladores globales cuestionan esa lógica y exigen un cambio de paradigma ético y científico.
El Real Decreto 1090/2015, que regula los ensayos clínicos con medicamentos en España, estableció criterios de protección reforzada para colectivos vulnerables. Esta norma reconoce la necesidad de equilibrar el riesgo con el beneficio potencial, garantizando de manera clara la supervisión ética y el consentimiento informado1. En el caso de embarazadas o en periodo de lactancia también se debe cumplir con el artículo 33 del Reglamento europeo 536/20142.
En los últimos tiempos, la normativa vigente está experimentando una transformación profunda. En 2023, el Consejo Internacional para la Armonización de los Requisitos Técnicos para los Productos Farmacéuticos de Uso Humano (ICH, por sus siglas en inglés) aprobó una guía de eficacia para establecer un marco que permita sumar a mujeres embarazadas y en periodo de lactancia en ensayos clínicos3.
A mediados de este año, la Agencia Europea de Medicamentos (AEM) presentó esa guía E21, un documento desarrollado en colaboración con reguladores y la industria farmacéutica de todo el mundo, cuyo periodo de consultas terminó el 15 de septiembre4.
Este texto aboga por que se incluya a embarazadas y lactantes en todos los ensayos clínicos de medicamentos que estén destinados a poblaciones que puedan concebir cuando esté justificado por un beneficio científico y clínico. El objetivo es generar datos que permitan a médicos y pacientes tomar decisiones basadas en evidencias, no en suposiciones o extrapolaciones4.
Protocolos más precisos
Las directrices de la guía ICH E21 no solo animan a incorporar a estos colectivos, sino que detallan los principios científicos, éticos y regulatorios que se deben cumplir para garantizar la seguridad de todos los participantes: embarazadas, lactantes, fetos y bebés. Esto implica diseñar3:
Por ejemplo, el desarrollo de una estrategia para recopilar datos relevantes para la lactancia se puede clasificar en los siguientes pasos5:
La adaptación de grupos de estudio para sumar a embarazadas en ensayos clínicos es una vía para avanzar en este ámbito6. Eso sí, al diseñar estos trabajos hay que preguntarse si7:
Las tendencias recientes muestran un impulso global sin precedentes. La Organización Mundial de la Salud (OMS) ha creado un grupo de trabajo mundial con la meta de lograr la inclusión de embarazadas y mujeres que amamantan en la investigación clínica para 20308.
Un análisis muestra que, de los ensayos clínicos registrados en el mundo durante la última década, solo el 4 % contaron con embarazadas, a pesar de que la mayoría de las mujeres toman al menos un medicamento prescrito mientras están encintas8.
Martina Penazzato, una de las responsables de investigación de la Red Global de Aceleradores para Formulaciones Pediátricas de la OMS (GAP-f), considera que “la inclusión ya no es una cuestión opcional y el paradigma debe cambiar”, ya que muchas mujeres con afecciones crónicas no saben si pueden continuar con sus tratamientos de manera segura cuando están embarazadas8.
Fuentes:
1. Boletín Oficial del Estado, Real Decreto 1090/2015, de 4 de diciembre, por el que se regulan los ensayos clínicos con medicamentos, los Comités de Ética de la Investigación con medicamentos y el Registro Español de Estudios Clínicos. https://www.boe.es/buscar/doc.php?id=BOE-A-2015-14082
2. Reglamento (UE) n °536/2014 del Parlamento Europeo y del Consejo, de 16 de abril de 2014, sobre los ensayos clínicos de medicamentos de uso humano https://eur-lex.europa.eu/legal-content/ES/TXT/?uri=CELEX:32014R0536
3. International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH), E21: Inclusion of Pregnant and Breast-feeding Individuals in Clinical Trials https://database.ich.org/sites/default/files/ICH_E21_Final_Concept_Paper_2023_1106_MCApproved.pdf
4. Agencia Europea de Medicamentos, New guideline on inclusion of pregnant and breastfeeding individuals in clinical trials https://www.ema.europa.eu/en/news/new-guideline-inclusion-pregnant-breastfeeding-individuals-clinical-trials
5. Agencia Europea de Medicamentos, ICH E21 Guideline on inclusion of pregnant and breastfeeding individuals in clinical trials https://www.ema.europa.eu/en/documents/other/ich-e21-guideline-inclusion-pregnant-breastfeeding-individuals-clinical-trials_en.pdf
6. Obstetric Medicine, Walking the walk to include pregnant participants in non-obstetric clinical trials: Insights from the SNAP Trial https://journals.sagepub.com/doi/10.1177/1753495X231163351
7. Journal of Obstetrics and Gynaecology Canada, Designing for Dyads: A multidisciplinary panel on inclusion of pregnant and lactating individuals and their infants in clinical trials https://www.jogc.com/article/S1701-2163(25)00357-3/fulltext
8. Organización Mundial de la Salud, Equidad y salud: la inclusión de las mujeres embarazadas y las mujeres que amamantan en los ensayos clínicos https://www.who.int/es/news/item/18-06-2025-equity-and-health–the-inclusion-of-pregnant-and-breastfeeding-women-in-clinical-trials